

ЛЕНВИМА® (ленватиниб)
Препарат Ленвима® показан к применению в монотерапии у взрослых пациентов с прогрессирующим или неоперабельным гепатоцеллюлярным раком, ранее не получавших системной терапии1.
Эффективность
Эффективность препарата ЛЕНВИМА® изучена в исследовании REFLECT — открытом многоцентровом исследовании III фазы2.
Первичная конечная точка в этом исследовании — общая выживаемость (ОВ)*.
Для препарата ЛЕНВИМА® подтверждена не меньшая ОВ vs сорафениб при нерезектабельном гепатоцеллюлярном раке (нГЦР) в первой линии терапии5.
ПОДРОБНАЯ ИНФОРМАЦИЯ О ДИЗАЙНЕ ИССЛЕДОВАНИЯ REFLECT

Исследование REFLECT: открытое многоцентровое исследование фазы III для подтверждения неменьшей эффективности2.
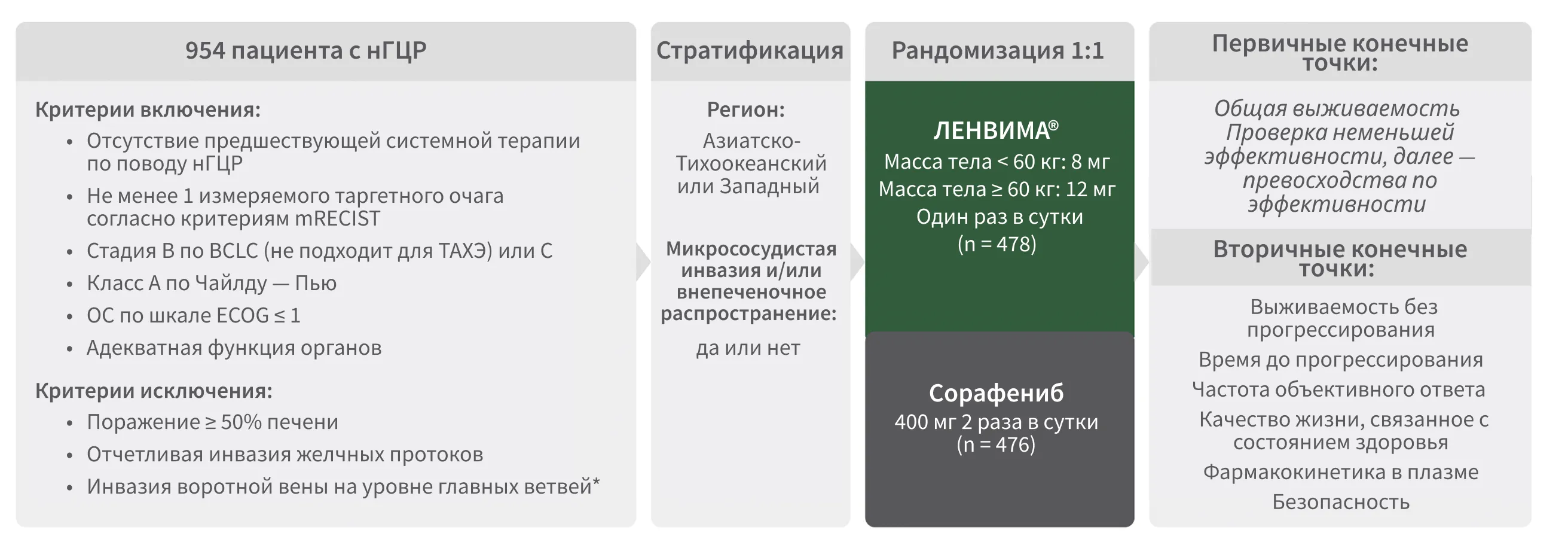
* По оценке исследователей. Апостериорные поисковые оценки опухолей с использованием критериев mRECIST и RECIST вер. 1.1 выполнялись на основании данных централизованного независимого анализа изображений2.
Для препарата ЛЕНВИМА® подтверждена не меньшая эффективность
в отношении ОВ vs сорафениб (13,6 и 12,3 месяца)2.
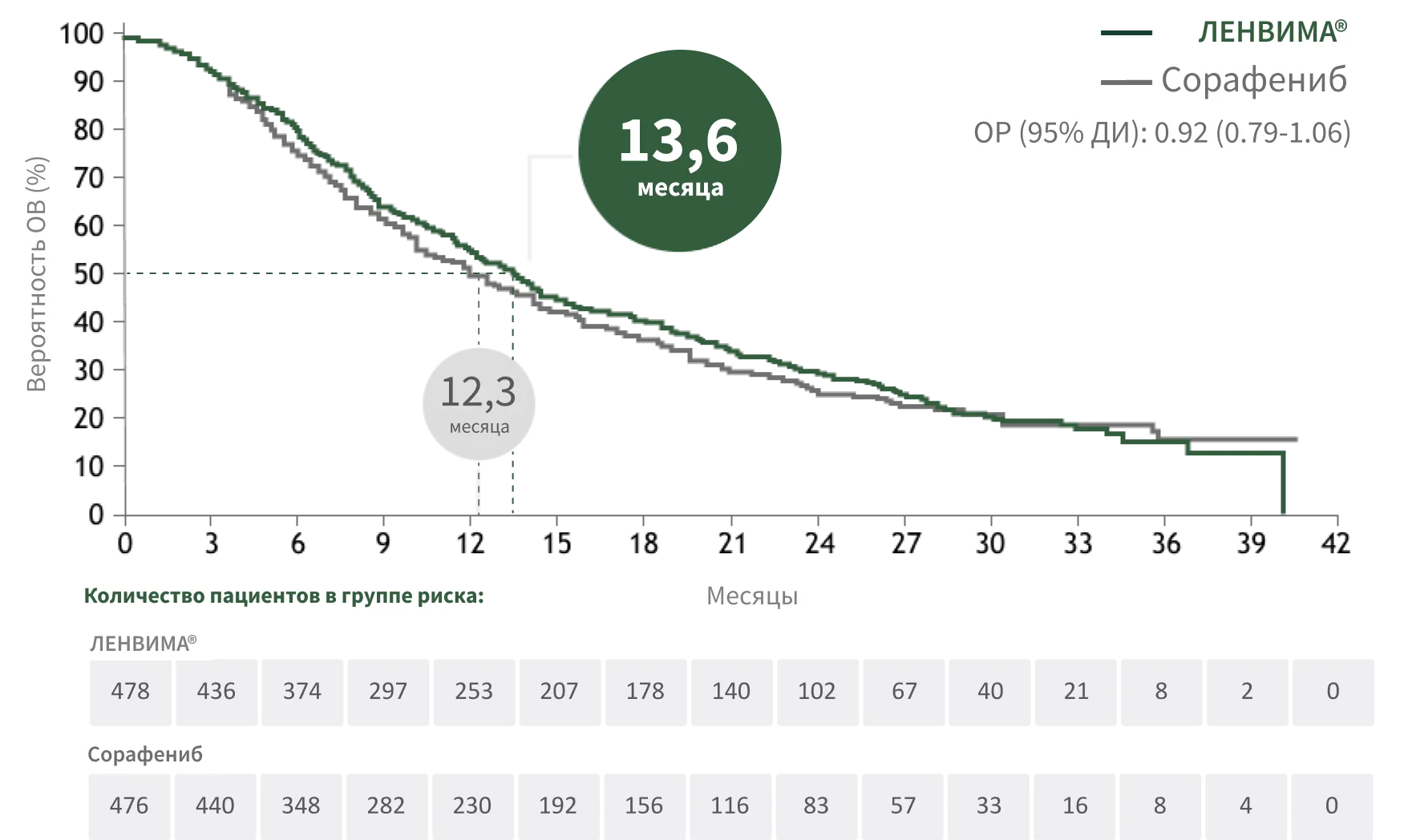
* Верхняя граница отношения рисков (ОР) для порога не меньшей эффективности установлена на уровне 1,08. Фактическая верхняя граница ОР: 1,06.
Вторичные конечные точки в исследовании REFLECT включали выживаемость без прогрессирования (ВБП), время до прогрессирования (ВДП), частоту объективного ответа (ЧОО), оценку качества жизни и фармакокинетических параметров2.
ЛЕНВИМА® vs сорафениб: УВЕЛИЧЕНИЕ МЕДИАНЫ ВБП В 2 РАЗА2.
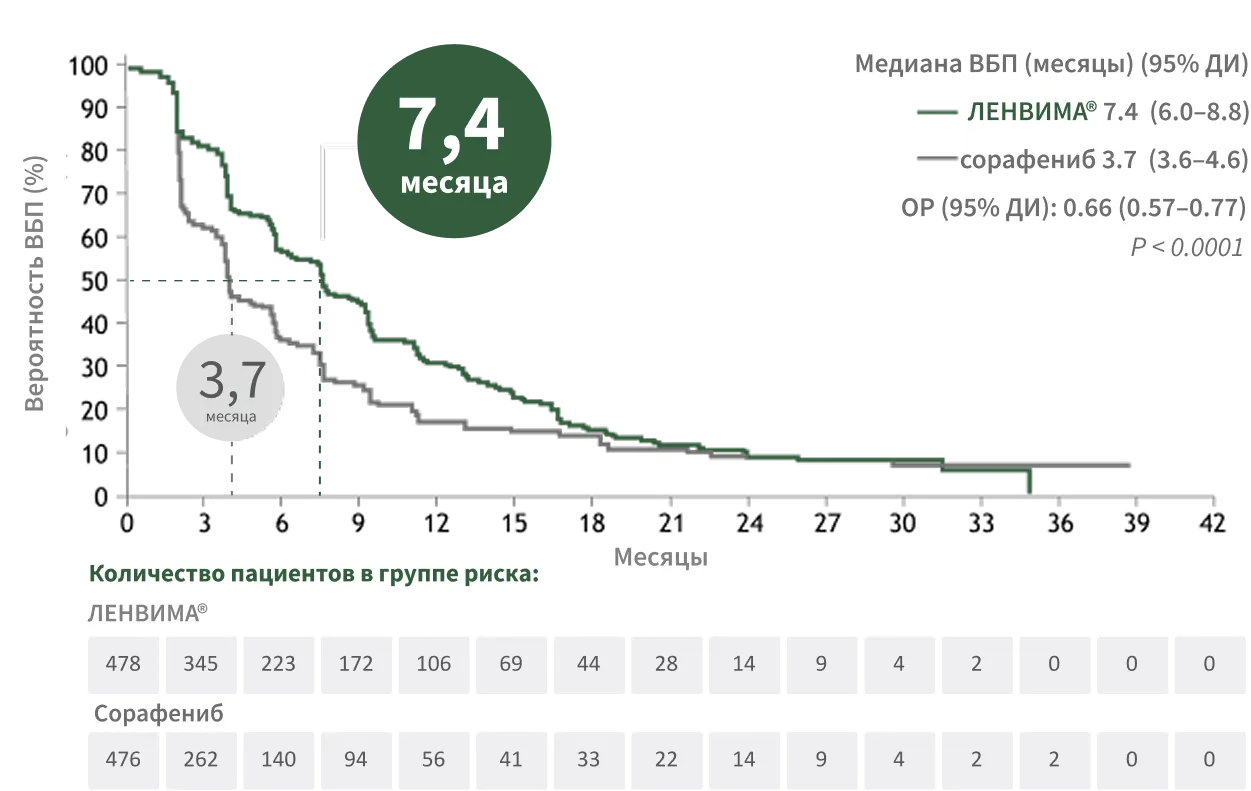
* По оценке исследователей. Апостериорные поисковые оценки опухолей с использованием критериев mRECIST и RECIST вер. 1.1 выполнялись на основании данных централизованного независимого анализа; показатели ВБП были схожими2.
ЛЕНВИМА® vs сорафениб: УВЕЛИЧЕНИЕ МЕДИАНЫ ВДП БОЛЕЕ ЧЕМ В 2 РАЗА2.
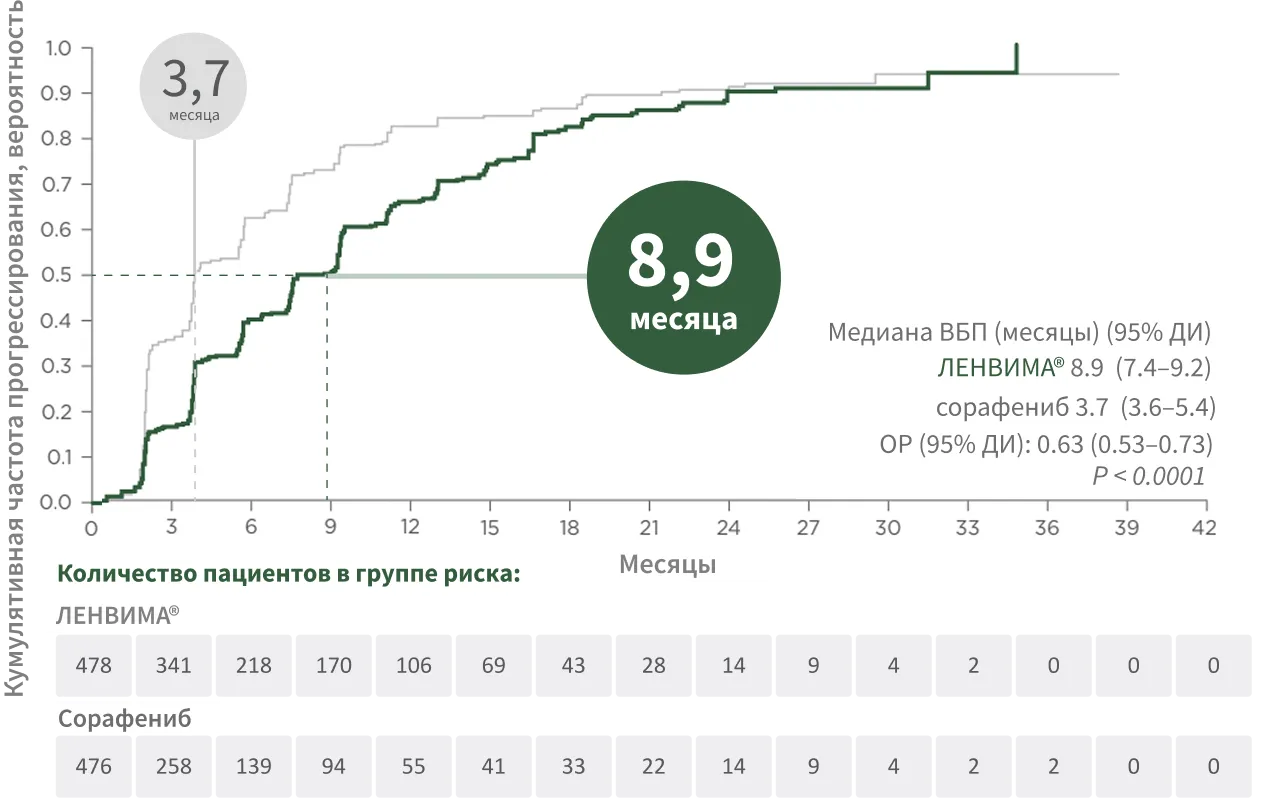
* По оценке исследователей. Апостериорные поисковые оценки опухолей с использованием критериев mRECIST и RECIST вер. 1.1 выполнялись на основании данных централизованного независимого анализа; показатели ВДП были схожими2.

Препарат ЛЕНВИМА® превосходит сорафениб
в отношении ЧОО
Подтверждено независимой оценкой изображений с использованием модифицированных критериев оценки ответа солидных опухолей mRECIST и RECIST вер. 1.12.
частота полных и частичных ОТВЕТОВ (N = 115) ПОЧТИ В 3 РАЗА ВЫШЕ vs СОРАФЕНИБ (N = 44) по данным независимой оценки изображений2.
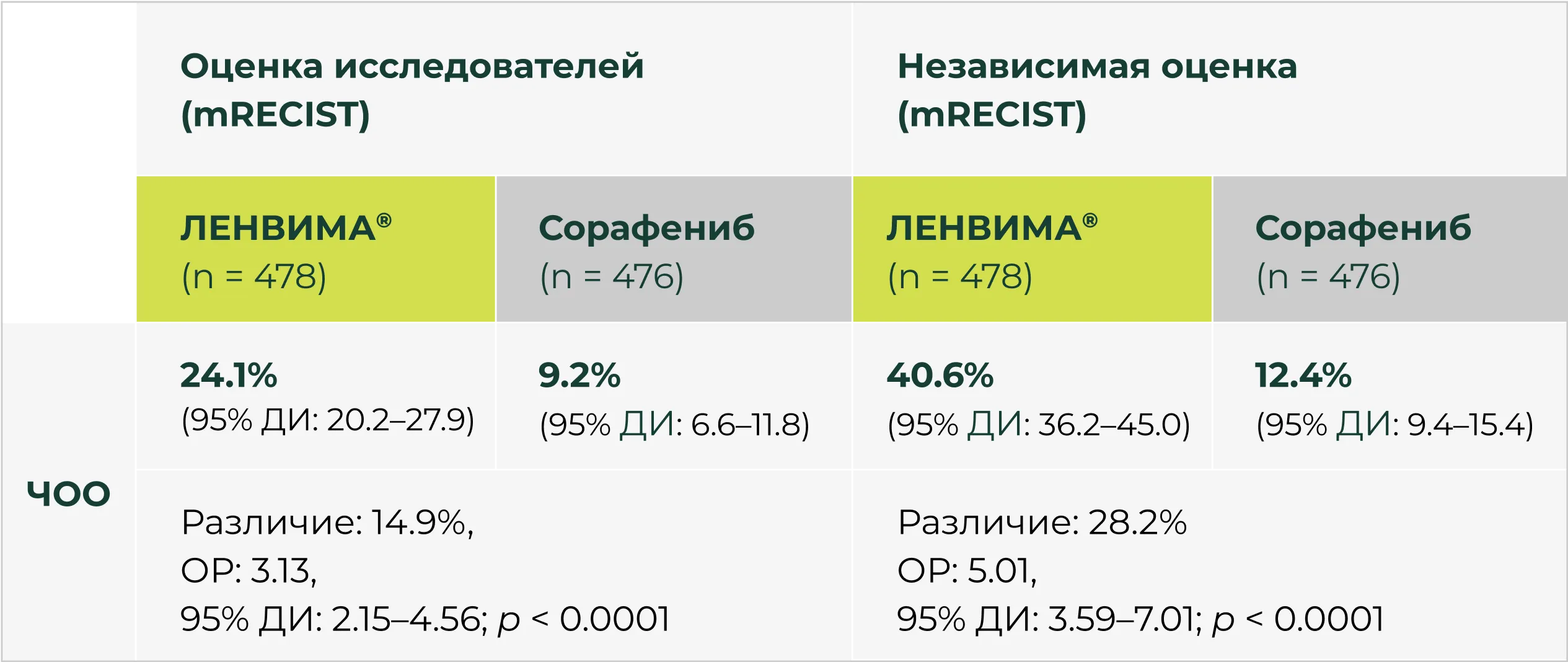
* По оценке исследователей (вторичная конечная точка). Апостериорные поисковые оценки опухолей выполнялись на основании данных централизованного независимого анализа2.
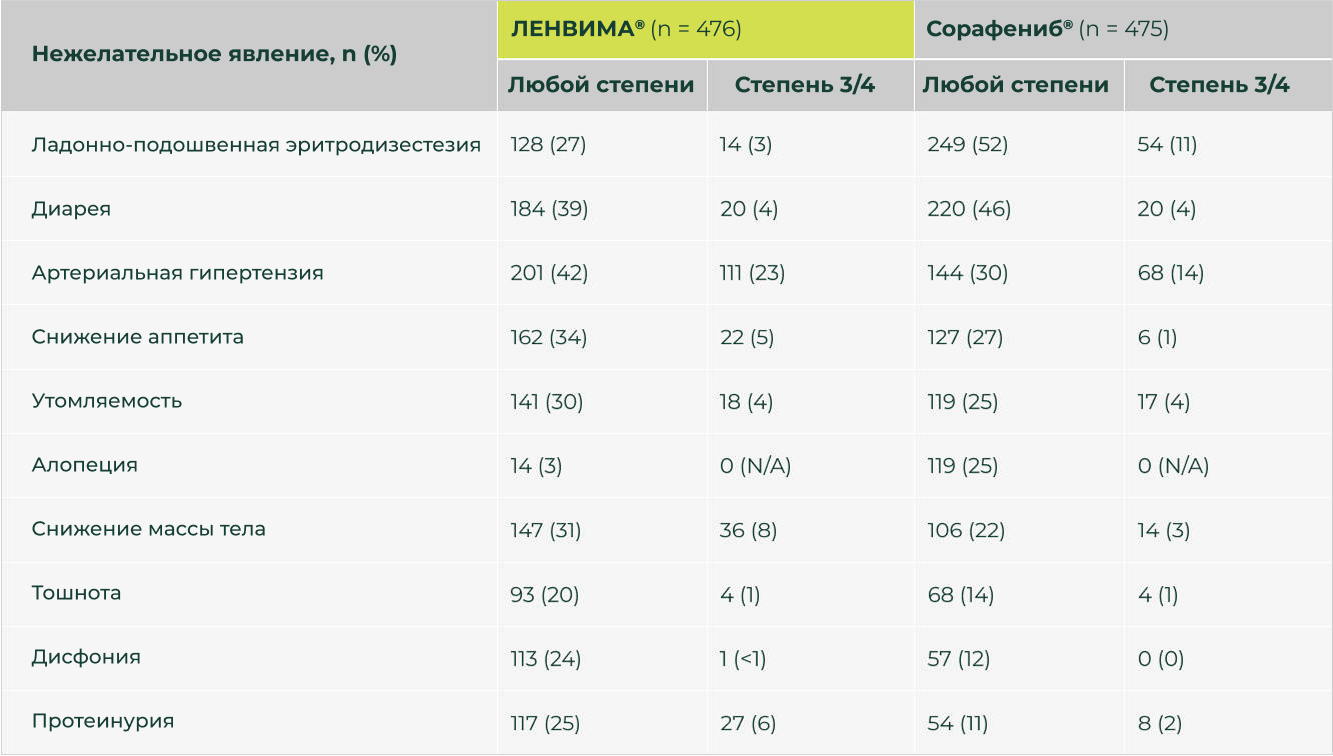
Безопасность и переносимость
По данным исследования REFLECT препарат ЛЕНВИМА® обладал управляемым профилем безопасности5.
Режим дозирования
Рекомендуемая доза препарата ЛЕНВИМА® при нГЦР составляет 8 мг один раз в сутки для пациентов с массой тела < 60 кг и 12 мг один раз в сутки для пациентов с массой тела ≥ 60 кг1.
Полную информацию о режиме дозирования см. в общей характеристике лекарственного препарата.
Информация о режиме дозирования представлена в таблице ниже1.
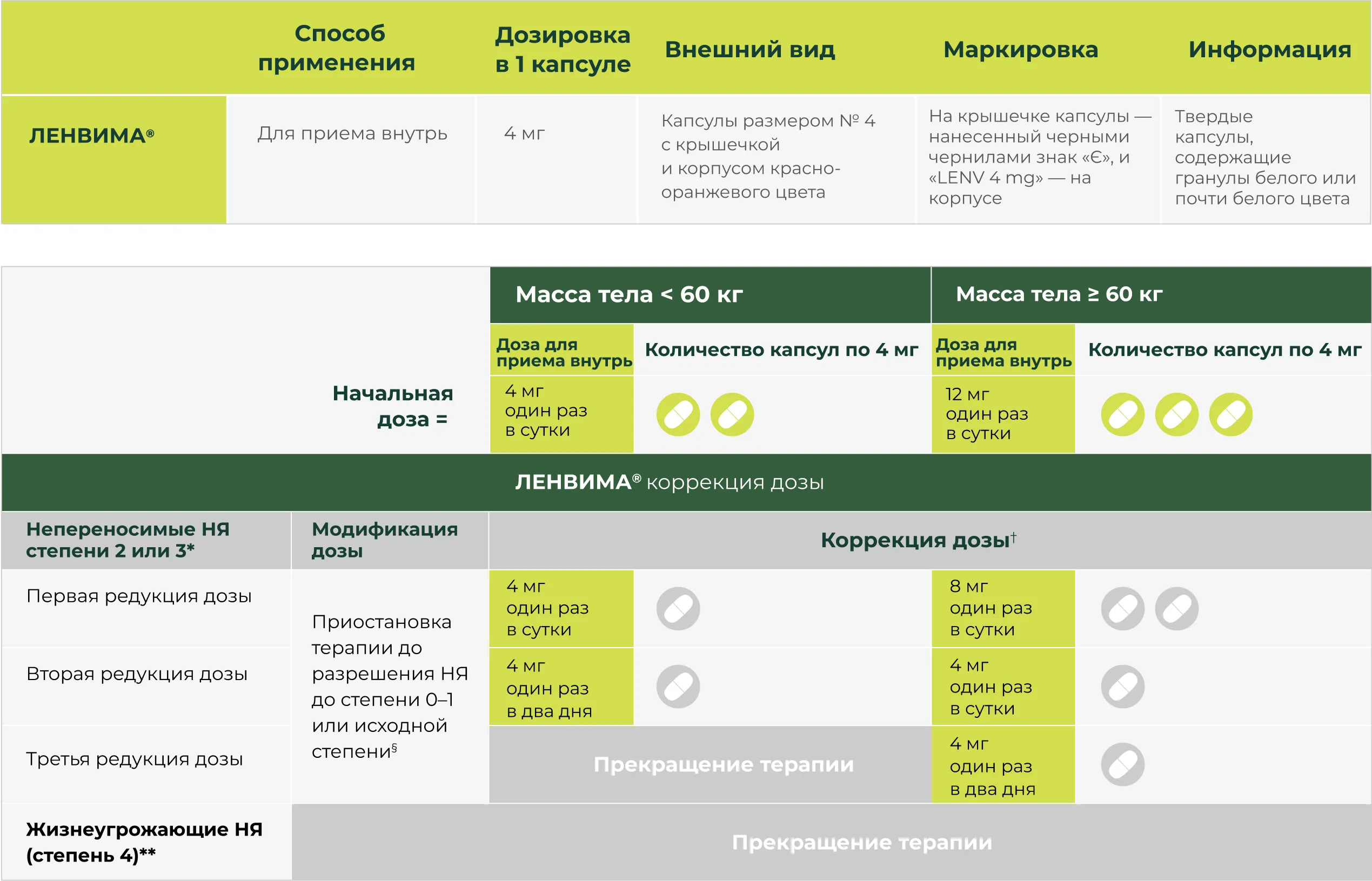
* До приостановки терапии или снижения дозы следует начать медикаментозное лечение тошноты, рвоты или диареи; желудочно-кишечные проявления токсичности требуют активного лечения, чтобы снизить риск развития нарушения функции почек или почечной недостаточности.
† Последовательное снижение дозы относительно предыдущего уровня (12 мг, 8 мг, 4 мг или 4 мг через день).
§ В случае гематологической токсичности лечение можно возобновить после уменьшения явления до 1–0 или исходной степени. При протеинурии возобновить терапию можно после того, как протеинурия снизится до уровня < 2 г / 24 ч.
** За исключением отклонений лабораторных показателей, признанных не опасными для жизни, которые следует вести как при степени 3.

ДЛЯ ПОЛУЧЕНИЯ БОЛЕЕ ПОДРОБНОЙ
ИНФОРМАЦИИ О ПРЕПАРАТЕ ЛЕНВИМА®
Свяжитесь с представителем компании Эйсай

ДИ — доверительный интервал; FGF — фактор роста фибробластов; FGFR — рецептор фактора роста фибробластов; ГЦР — гепатоцеллюлярный рак; ОР — отношение рисков; mRESIST — модифицированные критерии оценки ответа солидных опухолей; ОШ — отношение шансов; ЧОО — частота объективного ответа; ОВ — общая выживаемость; ВБП —выживаемость без прогрессирования; RESIST — критерии оценки ответа солидных опухолей; ИТК, ингибитор тирозинкиназы; ВДП — время до прогрессирования; нГЦР — нерезектабельный гепатоцеллюлярный рак; VEGF — фактор роста эндотелия сосудов; VEGFR — рецептор фактора роста эндотелия сосудов.
-
-
- 1. Общая характеристика лекарственного препарата (ОХЛП) Ленвима® (ленватиниб), капсулы. РУ ЛП-№(001897)-(РГ-RU).
- 2. Kudo M. et al. Lancet. 2018; 391(10126): 1163–1173.
-
