Гепатоцеллюлярная карцинома
Что такое гепатоцеллюлярная карцинома?
Гепатоцеллюлярная карцинома (ГЦК) — наиболее распространенная форма рака печени и один из самых агрессивных видов рака1-4. Наиболее значимым фактором риска развития ГЦК является наличие цирроза печени, независимо от его этиологии1. Цирроз присутствует у 70–90% пациентов с первичным раком печени1. К основным причинам развития относят хронические вирусные гепатиты В и С, а также употребление алкоголя1, 5.
Хотя подавляющее большинство случаев ГЦК возникает на фоне цирроза, рак печени также может развиться и в его отсутствии6. Неалкогольная жировая болезнь печени и неалкогольный стеатогепатит также относятся к факторам риска развития ГЦК7.
При ГЦК трансформация клеток печени в опухолевые может происходить по причине различного рода нарушений, в том числе наследственных, спонтанных генетических, а также под воздействием внешней среды. Данные нарушения могут влиять на различные гены, участвующие в процессе клеточного роста и деления, что приводит к нарушению пролиферации. Генетические изменения можно сгруппировать в два основных класса: преднеопластические (предшествующие образованию опухоли) и диспластические/неопластические (предзлокачественная и злокачественная стадии заболевания)8.
ГЦК — агрессивная опухоль, имеющая тенденцию к инвазии в систему воротной вены и другие сосуды, что может привести
к тромбозу воротной вены (ТВВ) и метастазированию9, 10.
ТВВ наблюдается у 10–60% пациентов с распространенной ГЦК
на момент постановки диагноза и связан с неблагоприятным прогнозом заболевания10.
Следствием склонности ГЦК к сосудистой инвазии является метастазирование опухоли. Чтобы метастазировать, опухолевые клетки должны оказаться в системном кровотоке, выжить в нем, избежав иммунного ответа, попасть в сосудистую сеть таргетного органа, выйти из сосудистого русла и образовать вторичный пролиферативный очаг. Несмотря на общепринятое представление о метастазировании как о распространении единичных циркулирующих опухолевых клеток, имеющиеся данные указывают на диссеминацию ГЦК в виде многоклеточных кластеров9.
Гепатоцеллюлярная карцинома
Эпидемиология
В 2020 году рак печени занимал 6-е место по распространенности среди онкологических заболеваний в мире4: чаще встречается у мужчин (5-е место по распространенности) по сравнению с женщинами (9-е место)11.
В 2020 году в Европе рак печени занимал 13-е место по распространенности среди всех онкологических заболеваний11. По оценкам, было зарегистрировано 87 630 новых случаев (58 079 у мужчин и 29 551 у женщин)11.
В 2020 году почти 45% случаев рака печени во всем мире приходилось на Китай11.
В 2020 году рак печени стал второй по значимости причиной смерти от онкологических заболеваний среди мужчин и шестой среди женщин в мире, унеся 830 180 жизней11.
В период с 2005 по 2009 год пятилетняя выживаемость взрослых пациентов в развитых и развивающихся регионах оставалась низкой: 15–18% в Северной Америке,
4–27% в Азии, 5–20% в Европе и 15–17% в Океании12.
Продолжительность жизни при ГЦК зависит от стадии заболевания на момент постановки диагноза13.
Стадирование гепатоцеллюлярной карциномы
Цель системы стадирования — оценить прогноз для конкретного пациента, чтобы можно было подобрать соответствующую терапию.
До сих пор разработка и использование единой общепринятой стандартизированной системы классификации ГЦК является крайне актуальным вопросом14.
Современные системы стадирования ГЦК учитывают как характеристики опухоли, так и степень дисфункции печени, поскольку прогноз при ГЦК зависит от обоих факторов14.
Шкала Чайлд — Пью является наиболее широко используемой системой для качественной оценки функции печени у пациентов
с циррозом и включена в различные системы стадирования ГЦК.
К ограничениям этой системы стадирования относят субъективный характер клинической оценки асцита и энцефалопатии, а также ежедневные колебания и вариации лабораторных показателей14.
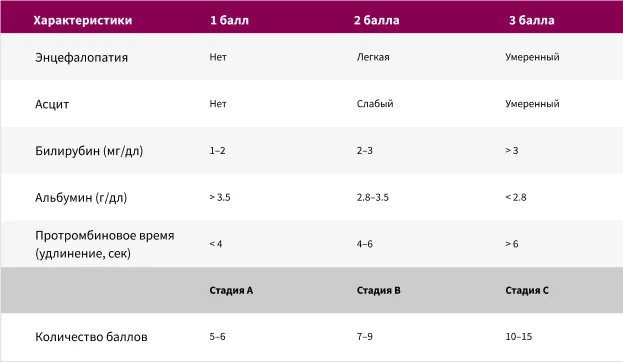
Таблица 1. Шкала Чайлда — Туркотта — Пью. По материалам Subramaniam S. et al. Chin Clin Oncol. 2013; 2: 33.14.
Система стадирования Окуда — это прогностическая система оценки, которая учитывает характеристики опухоли и степень дисфункции печени.
Пациентов оценивают на основании наличия четырех факторов: размеры опухоли (> 50% печени), асцит, альбумин (< 3 г/дл) и билирубин (> 3 мг/дл). Затем результаты стратифицируют на три стадии в зависимости от количества присутствующих факторов14.
Шкала Окуда была включена в формулы других систем стадирования в качестве критерия оценки14. Примером является Классификация рака печени
Барселонской клиники (BCLC). Впервые опубликованная в 1999 году, она является наиболее широко используемой системой стадирования ГЦК, поскольку учитывает множество факторов14.
Данные факторы включают клинический статус, стадию по Окуда, характеристики опухоли и функцию печени14-16. Если сравнивать
с системой стадирования Окуда, стадия D по BCLC эквивалентна стадии III по Окуда14.

Таблица 2. Стадирование по Окуда. По материалам Subramaniam S. et al. Chin Clin Oncol. 2013; 2: 33.14.


* В обновленной версии BCLC 2018 г. шкала Чайлда — Пью больше не применяется для оценки функции печени. Декомпенсация заболевания печени (желтуха, асцит, энцефалопатия) указывает на печеночную недостаточность, независимо от оценок по шкале Чайлда — Пью или модели для оценки терминальной стадии заболевания печени (MELD)16.
Таблица 3. Система стадирования BCLC. По материалам Adhoute X. et al. World J Hepatol. 2016; 8: 703–715.15.
Система стадирования BCLC связана с алгоритмом лечения16, 17 и рекомендована EASL-EORTC и Американской ассоциацией
по изучению болезней печени (AASLD) для выбора тактики лечения18. Рекомендации по лечению не являются строгими и адаптируются
индивидуально, учитывая доступные ресурсы19. Стадии BCLC и подход к лечению, согласно последнему обновлению классификации в 2022 году,
а также предполагаемая выживаемость по стадиям показаны ниже16.
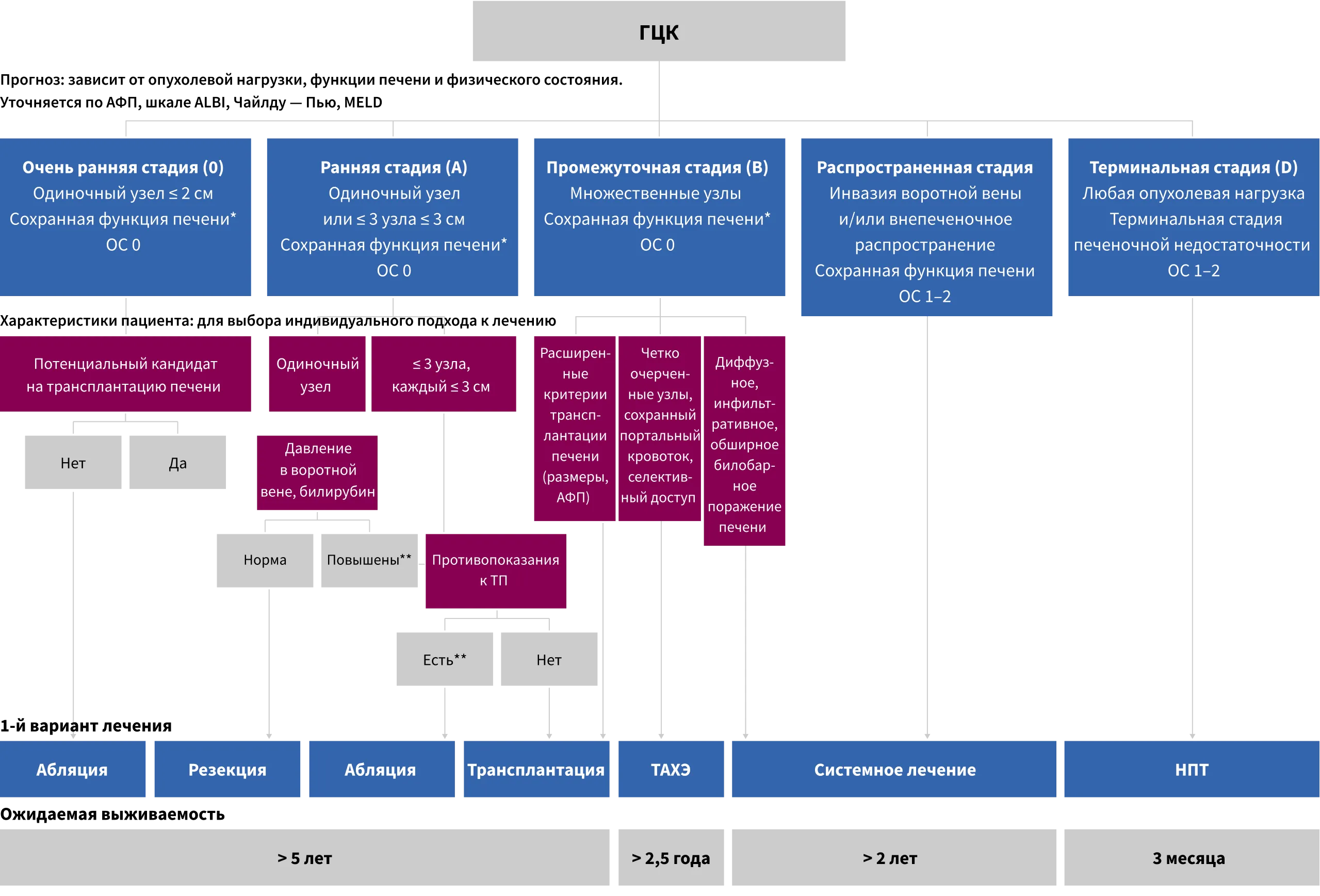
* За исключением пациентов с опухолевой нагрузкой, приемлемой для трансплантации.
** Резекция может рассматриваться при одиночной периферической ГЦК с адекватным объемом остаточной печени.
Таблица 4. Классификация рака печени Барселонской клиники. По материалам Reig M., et al. J Hepatol. 2022; 76(3): 681–693.16.
Клинические проявления и симптомы гепатоцеллюлярной карциномы
Симптомы ГЦК часто не проявляются до тех пор, пока заболевание не достигнет поздних стадий, и их может быть трудно отличить
от симптомов,
связанных с основным хроническим заболеванием печени (циррозом)8. Регулярный мониторинг пациентов
с хроническими заболеваниями печени,
которые относятся к группе риска по развитию ГЦК, с целью выявления опухолевых проявлений и симптомов может способствовать ранней диагностике рака печени8.
- Гепатомегалия (увеличение печени)
- Боль или дискомфорт в животе
- Желтуха
- Асцит (скопление жидкости в брюшной полости)
- Общие симптомы (утомляемость, недомогание, лихорадка, снижение массы тела)
- Кровотечение из органов пищеварения или в брюшную полость
- Печеночная энцефалопатия (поражение головного мозга, вызванное дисфункцией печени)

Типы гепатоцеллюлярной карциномы
Ранняя диагностика ГЦК, когда опухолевый объем характеризуется как небольшой (< 2 см), критически важна для снижения риска рецидива или прогрессирования заболевания18.
Несмотря на то, что при распространенном раке печени радикальное лечение чаще всего невозможно, длительный период без прогрессирования предоставляет возможность для раннего вмешательства20.
В этот период роста опухоль может быть обнаружена, но все еще протекает бессимптомно8.
Усовершенствование методов диагностики и визуализации увеличило частоту выявления ГЦК на ранних стадиях.
Согласно рекомендациям EASL-EORTC, диагноз ГЦК ставится на основании данных неинвазивных методов обследования или результатов патоморфологического исследования.
ГЦК характеризуется специфическими характеристиками, которые определяются
с помощью усовершенствованных методов визуализации18.


Хотя визуальных методов в большинстве случаев достаточно для диагностики ГЦК, в ряде ситуаций требуется проведение более инвазивных тестов20.
Патоморфологическая диагностика ГЦК должна соответствовать рекомендациям Международной консенсусной группы и включать необходимые гистологические и иммуногистохимические исследования18.
Основным патологическим признаком ГЦК является инвазия стромы, однако на ранней стадии заболевания ее можно не заметить в материале биопсии18.
Анализы на опухолевые биомаркеры, включая альфа-фетопротеин, глипикан-3 (GPC3), белок теплового шока 70 (HSP70) и глутаминсинтетазу (GS), могут помочь в диагностике рака печени.
Согласно рекомендациям Международной консенсусной группы по гепатоцеллюлярной неоплазии, необходимо наличие положительного результата для по крайней мере двух маркеров из трех (GPC3, HSP70 или GS) для диагностики ГЦК21.
Больше узнать о лечении
ЛЕНВИМА® при ГЦКAASLD — Американская ассоциация по изучению болезней печени; АФП — альфа-фетопротеин; ALBI — альбумин-билирубин; BCLC — Барселонская клиника по лечению рака печени; НПТ — наилучшая поддерживающая терапия; EASL-EORTC — Европейская ассоциация по изучению печени — Европейская организация по исследованию и лечению рака; ECOG — Восточная объединенная онкологическая группа; GPC3 — глипикан-3; GS — глутаминсинтетаза; ГЦК — гепатоцеллюлярная карцинома; HSP70 — белок теплового шока 70; ТП — трансплантация печени; MELD — модель для оценки терминальной стадии заболевания печени; ОС — общее состояние; ТВВ — тромбоз воротной вены; ТАХЭ —трансартериальная химиоэмболизация.
-
-
- 1. Herbst D. et al. Clin Liver Dis. 2013; 1: 180–182.
- 2. Torre L. et al. Cancer Epidemiol Biomarkers Prev. 2016; 25: 16–27.
- 3. What is liver cancer? ACS. Available at: https://www.cancer.org/cancer/liver-cancer/about/what-is-liver-cancer.html (Accessed July 2023).
- 4. Liver cancer fact sheet. 2020. Available at: https://gco.iarc.fr/today/data/factsheets/cancers/11-Liver-fact-sheet.pdf (Accessed July 2023).
- 5. NIDDK. Symptoms and Causes of Cirrhosis. Available at: https://www.niddk.nih.gov/health-information/liver-disease/cirrhosis/symptoms-causes (Accessed July 2023).
- 6. Gaddikeri S. et al. Am J Roentgenol. 2014; 203: W34–W47.
- 7. Smeuninx B. et al. Cancers (Basel). 2020; 12(7): 1714.
- 8. Trevisani F. et al. Carcinogenesis. 2008; 29: 1299–1305.
- 9. Sugino T. et al. Clin Exp Metastasis. 2008; 25: 835–841.
- 10. Chan S. et al. World J Gastroenterol. 2016; 22: 7289–7300.
- 11. WHO. Cancer Today statistics. 2020. Available at: https://gco.iarc.fr/today/online-analysis-table?v=2018&mode=cancer&mode_population=continents&population=900&populations=900&key=asr&sex=0&cancer=39&type=0&statistic=5&prevalence=0&population_group=0&ages_group%5B%5D=0&ages_group%5B%5D=17&group_cancer=1&include_nmsc=1&include_nmsc_other=1 (Accessed July 2023).
- 12. Allemani C. et al. Lancet. 2015; 385: 977–1010.
- 13. SEER. Cancer Statistics Review, 2013–2019. Available at: https://seer.cancer.gov/statistics-network/explorer/application.html?site=35&data_type=4&graph_type=5&compareBy=stage&chk_stage_104=104&chk_stage_105=105&chk_stage_106=106&series=9&sex=1&race=1&age_range=1&advopt_precision=1&advopt_show_ci=on&hdn_view=0&advopt_display=2#graphArea (Accessed July 2023).
- 14. Subramaniam S. et al. Chin Clin Oncol. 2013; 2: 33.
- 15. Adhoute X. et al. World J Hepatol. 2016; 8: 703–715.
- 16. Reig M., et al. J Hepatol. 2022; 76(3): 681–693.
- 17. Forner A. et al. Lancet. 2018; pii: S0140-6736(18)30010–2.
- 18. EASL-EORTC Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol. 2018; 69: 182–236.
- 19. Prasad M. et al. J Natl Compr Canc Netw. 2014; 12: 1183–1190.
- 20. Bruix J. et al. Gastroenterol. 2016; 150: 835–853.
- 21. International Consensus Group for Hepatocellular Neoplasia. Hepatology. 2009; 49: 658–664.
-
